3 - Termoquímica
Artículos de esta sección
-
Solución
El sulfuro de carbono reacciona con el oxígeno según:
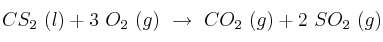
Sabiendo que su
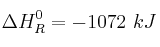 :
:a) Calcula la entalpía de formación del
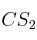 .
.b) Halla el volumen de
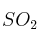 emitido a la atmósfera, a 1 atm y 298 K, cuando se ha liberado una energía de 6000 kJ.
emitido a la atmósfera, a 1 atm y 298 K, cuando se ha liberado una energía de 6000 kJ.Datos (en kJ/mol):
![\Delta H^0_f[CO_2(g)] = -393,5 \Delta H^0_f[CO_2(g)] = -393,5](local/cache-TeX/65e768b96c9d00dc4817fb29e68b8406.png) ;
; ![\Delta H^0_f[SO_2(g)] = -296,4 \Delta H^0_f[SO_2(g)] = -296,4](local/cache-TeX/7c7985afaf3d6923efd260d25591fbd5.png)
-
Solución
El sulfuro de cinc reacciona con el oxígeno según:
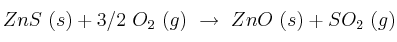
Halla la energía que se desprende cuando reaccionan 17,6 g de sulfuro de cinc en condiciones estándar.
Datos (en kJ/mol):
![\Delta H^0_f[ZnS(s)] = -184,1 \Delta H^0_f[ZnS(s)] = -184,1](local/cache-TeX/467ba76e943c60697d0981d778eb465e.png) ;
; ![\Delta H^0_f[SO_2(g)] = -70,9 \Delta H^0_f[SO_2(g)] = -70,9](local/cache-TeX/025bf4b78e373573abf8ea9eaebabe66.png) ;
; ![\Delta H^0_f[ZnO(s)] = -349,3 \Delta H^0_f[ZnO(s)] = -349,3](local/cache-TeX/314754e7a5bbca7668768d5eebf30b45.png)
-
Solución
A partir de la reacción de la fotosíntesis que realizan las plantas verdes:
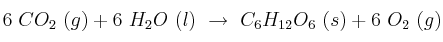
y sabiendo que
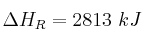 :
:a) ¿Qué volumen de oxígeno, medido en condiciones estándar, se produce por cada gramo de glucosa formado?
b) Qué energía se requiere en ese proceso?
-
Solución
Calcula la variación de entalpía de la fermentación de la glucosa según la reacción:
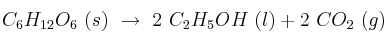
si las entalpías de combustión de la glucosa y del etanol son -2813 kJ/mol y -1367 kJ/mol, respectivamente.
-
Solución
Sabiendo que los calores de combustión de
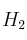 (g), C (s) y
(g), C (s) y 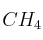 (g) son respectivamente: -68,40 ; -95,29 y -200,10 kcal/mol:
(g) son respectivamente: -68,40 ; -95,29 y -200,10 kcal/mol:a) Escribe las ecuaciones termoquímicas que describen los tres procesos.
b) Calcula el calor de formación del metano. ¿Es un proceso endotérmico? ¿Por qué?
-
Solución
La entalpía de combustión de un hidrocarburo gaseoso
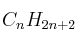 es -2220 kJ/mol. Calcule:
es -2220 kJ/mol. Calcule:a) La fórmula molecular de este hidrocarburo.
b) La energía desprendida en la combustión de 50 L de este gas, medidos a 25 ºC y 1 atm.
c) La masa de
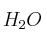 (l) que se obtendrá en la combustión anterior.
(l) que se obtendrá en la combustión anterior.Datos: R = 0,082 atm·L/K·mol ; Entalpías de formación (kJ/mol):
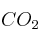 (g) = -393 ;
(g) = -393 ; 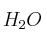 (l) = -286 ;
(l) = -286 ; 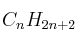 = -106 ; Masas atómicas: H = 1 ; O = 16.
= -106 ; Masas atómicas: H = 1 ; O = 16.
0 | 10


