SELECTIVIDAD Junio 2013
Artículos de esta sección
-
Formula o nombra los siguientes compuestos:Solución
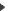 a) Hidróxido de paladio(II)
a) Hidróxido de paladio(II)
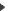 b) Ácido sulfúrico
b) Ácido sulfúrico
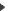 c) Ácido 2-aminopropanoico
c) Ácido 2-aminopropanoico
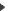 d)
d) 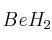
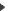 e)
e) 
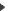 f)
f) 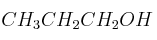
-
Solución
Para los siguientes elementos Na, P, S y Cl, diga razonadamente cuál es:
 a) El de menor energía de ionización.
a) El de menor energía de ionización.
 b) El de mayor afinidad electrónica.
b) El de mayor afinidad electrónica.
 c) El de mayor radio atómico.
c) El de mayor radio atómico. -
Solución
Justifica la veracidad o falsedad de las siguientes afirmaciones:
a) Como el producto de solubilidad del cloruro de plata es
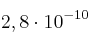 , la solubilidad en agua de esta sal
, la solubilidad en agua de esta sal 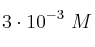 .
.b) En toda disolución saturada de hidróxido de magnesio se cumple:
![[OH^-][Mg^{2+}]^2 = K_s [OH^-][Mg^{2+}]^2 = K_s](local/cache-TeX/028969586ce6c819c724a4798bd0dfd9.png) .
.c) Todos los hidróxidos poco solubles se hacen aún más insolubles en medio básico.
-
Solución
La fórmula molecular del azúcar común o azúcar de mesa (sacarosa) es
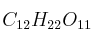 . Indique razonadamente si un mol de sacarosa contiene:
. Indique razonadamente si un mol de sacarosa contiene:a) 144 g de carbono.
b) 18 mol de átomos de carbono.
c)
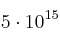 átomos de carbono.
átomos de carbono. -
Solución
Una muestra de un mineral que contiene cobre, además de impurezas inertes, se disuelve con ácido nítrico concentrado según siguiente reacción sin ajustar:
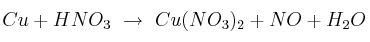
a) Ajusta por el método del ión-electrón la ecuación molecular.
b) Calcula el contenido en cobre de la muestra si 1 g de la misma reacciona totalmente con 25 mL de ácido nítrico 1 M.
Masa atómica del Cu = 63,5.
-
Solución
En la reacción del oxígeno molecular con cobre para formar óxido de cobre(II) se desprende 2,3 kJ por cada gramo de cobre que reacciona, a 298 K y 760 mm Hg. Calcula:
a) La entalpía de formación del óxido de cobre(II).
b) El calor desprendido a presión constante cuando reaccionan 100 L de oxígeno, medidos a 1,5 atm y 27 ºC.
Datos: R = 0,082
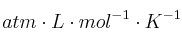 ; Masa atómica del Cu = 63,5.
; Masa atómica del Cu = 63,5. -
Formula o nombra los siguientes compuestos: a) Peróxido de bario ; b) Hidróxido de magnesio ; c) Etanamida ; d)Solución
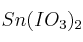 ; e)
; e) 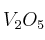 ; f)
; f) 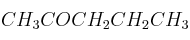
-
Solución
Dadas las siguientes sustancias, Cu, CaO y
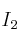 , indica razonadamente:
, indica razonadamente:a) Cuál conduce la electricidad en estado líquido pero es aislante en estado sólido.
b) Cuál es un sólido que sublima fácilmente.
c) Cuál es un sólido que no es frágil y se puede estirar en hilos o láminas.
-
Solución
Para la reacción
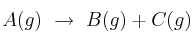 el valor de la constante de velocidad a una cierta temperatura es
el valor de la constante de velocidad a una cierta temperatura es 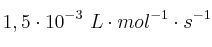 .
.a) ¿Cuál es el orden de la reacción?
b) ¿Cuál es la ecuación de velocidad?
c) A esa misma temperatura, ¿cuál será la velocidad de la reacción cuando la concentración de A sea 0,242 M?
-
Solución
Sea la transformación química
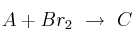 . Si reacciona 1 mol de
. Si reacciona 1 mol de 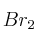 indica, justificando la respuesta, si las siguientes afirmaciones son verdaderas o falsas:
indica, justificando la respuesta, si las siguientes afirmaciones son verdaderas o falsas:a) Cuando A es 1 mol de
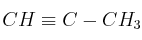 el producto C no presenta isomería geométrica.
el producto C no presenta isomería geométrica.b) Cuando A es 1 mol de
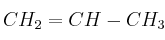 el producto C presenta isomería geométrica.
el producto C presenta isomería geométrica.c) Cuando A es 0,5 mol de
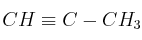 el producto C no presenta isomería geométrica.
el producto C no presenta isomería geométrica.
0 | 10


