SELECTIVIDAD Septiembre 2011
Artículos de esta sección
-
Formula o nombra los compuestos siguientes: a) Óxido de calcio ; b) Ácido bórico ; c) Hepta-2,4-dieno ; d)Solución
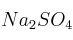 ; e)
; e) 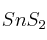 ; f)
; f) 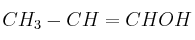
-
Solución
Considera los elementos Be, O, Zn y Ar.
a) Escribe las configuraciones electrónicas de los átomos anteriores.
b) ¿Cuántos electrones desapareados presentan cada uno de esos átomos?
c) Escribe las configuraciones electrónicas de los iones más estables que puedan formar.
-
Solución
Dados los valores de potencial de reducción estándar de los sistemas:
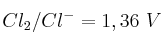 ;
; 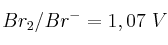 y
y 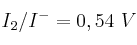 , indica razonadamente:
, indica razonadamente:a) ¿Cuál es la especie química más oxidante entre las mencionadas anteriormente?
b) ¿Es espontánea la reacción entre el cloro molecular y el ion yoduro?
c) ¿Es espontánea la reacción entre el yodo y el ion bromuro?
-
Solución
La reacción de hidrogenación del buta-1,3-dieno para dar butano es
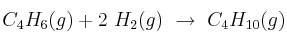 . Calcula la entalpía de la reacción a 25 ºC y en condiciones estándar:
. Calcula la entalpía de la reacción a 25 ºC y en condiciones estándar:a) A partir de la entalpía de formación del agua y de las entalpías de combustión del buta-1,3-dieno y del butano.
b) A partir de las entalpías de enlace.
Datos:
![\Delta H_C^0[C_4H_6(g)] = -2540,2\ kJ/mol \Delta H_C^0[C_4H_6(g)] = -2540,2\ kJ/mol](local/cache-TeX/8def700d5e629e0012f77d6d53d85868.png) ;
; ![\Delta H_C^0[C_4H_{10}(g)] = -2877,6\ kJ/mol \Delta H_C^0[C_4H_{10}(g)] = -2877,6\ kJ/mol](local/cache-TeX/7c3b4856f15a580f055b64f06c3d1aad.png) ;
; ![\Delta H_f^0[H_2O(l)] = -285,6\ kJ/mol \Delta H_f^0[H_2O(l)] = -285,6\ kJ/mol](local/cache-TeX/ab792c53203f068d97f6bbb9308c00b3.png) . Entalpías de enlace (kJ/mol): (C-C) = 348,2 ; (C=C) = 612,9 ; (C-H) = 415,3 ; (H-H) = 436,4.
. Entalpías de enlace (kJ/mol): (C-C) = 348,2 ; (C=C) = 612,9 ; (C-H) = 415,3 ; (H-H) = 436,4. -
Solución
A cierta temperatura el producto de solubilidad en agua del AgI es
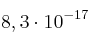 . Para esa temperatura, calcula la solubilidad molar del compuesto en:
. Para esa temperatura, calcula la solubilidad molar del compuesto en:a) Una disolución 0,1 M de
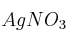
b) Una disolución de ácido yodhídrico de pH = 2
-
Formula o nombra los compuestos siguientes: a) Sulfuro de manganeso(III) ; b) Hidrogenocarbonato de cadmio ; c) Ácido benzoico ; d)Solución
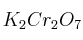 ; e)
; e) 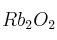 ; f)
; f) 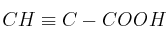
-
Solución
Con relación a los compuestos benceno (
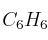 ) y acetileno (
) y acetileno (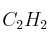 ), ¿cuáles de las siguientes afirmaciones son ciertas? Razone las respuestas.
), ¿cuáles de las siguientes afirmaciones son ciertas? Razone las respuestas.a) Los dos tienen la misma fórmula empírica.
b) Los dos tienen la misma fórmula molecular.
c) Los dos tienen la misma composición centesimal.
-
Solución
Dadas las moléculas
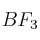 ,
, 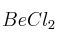 y
y 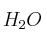 :
:a) Escribe las estructuras de Lewis de las mismas.
b) Explique su geometría mediante la Teoría de Repulsión de los Pares de Electrones de la Capa de Valencia.
c) Indique la hibridación del átomo central.
-
Solución
Razona si son verdaderas o falsas las siguientes afirmaciones:
a) Dos disoluciones acuosas de pH = 2 de distintos ácidos tienen la misma concentración de ácido.
b) Una base débil es aquella cuyas disoluciones acuosas siempre son diluidas.
c) La disociación de un ácido fuerte en agua es prácticamente total.
0 | 10


