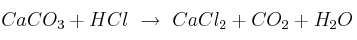Portada del sitio > Acc. Univ. Mayores 25 - QUIMICA > EXÁMENES RESUELTOS > UNED 2011 Septiembre (Química)
UNED 2011 Septiembre (Química)
Artículos de esta sección
-
¿Cuál es la temperatura final de un gas contenido en un recipiente cerrado, inicialmente a 25 ºC y 453 mm Hg, si se dobla la presión? Cita la ley que aplicas.Solución
-
Solución
El estroncio, tal como existe en estado natural, está compuesto de cuatro isótopos que se enumeran a continuación con sus abundancias relativas expresadas en porcentajes de átomos. A partir de estos datos, calcula el peso atómico del estroncio en estado natural.
Isótopos:
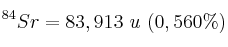 ;
; 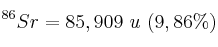 ;
; 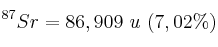 ;
; 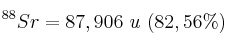
-
Determina la concentración de iones hidronio e iones hidroxilo de una disolución cuyo pH es igual a 5.Solución
-
Solución
Clasifica cada una de las siguientes reacciones como ácido-base y oxidación-reducción, razonando detalladamente la respuesta:
a)
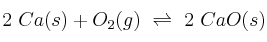
b)
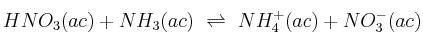
c)
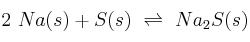
-
Solución
Se tratan 250 g de
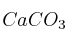 con ácido clorhídrico y se desea saber: a) la cantidad de HCl en peso necesaria; b) ¿qué cantidad de
con ácido clorhídrico y se desea saber: a) la cantidad de HCl en peso necesaria; b) ¿qué cantidad de 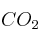 en peso se obtendrá?; c) ¿qué volumen de
en peso se obtendrá?; c) ¿qué volumen de 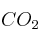 se obtendrá en condiciones normales?
se obtendrá en condiciones normales?Pesos atómicos: C=12 ; O=16 ; H=1 ; Cl=35,4 ; Ca=40. La reacción sin ajustar es: