Portada del sitio > Química - 1Bach > Q03 - Leyes Fundamentales de la Química
Q03 - Leyes Fundamentales de la Química
Ejercicios de Ampliación
Artículos de esta sección
-
El plomo se combina con el oxígeno para dar
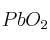 ; si se hace reaccionar una muestra de 12,5 g que contiene plomo y otras sustancias inertes y en la reacción se producen 11,544 g de óxido de plomo, gastándose para ello 1,544 g de oxígeno, ¿qué porcentaje de plomo contiene la muestra, suponiendo que reacciona todo el plomo presente en la misma?
; si se hace reaccionar una muestra de 12,5 g que contiene plomo y otras sustancias inertes y en la reacción se producen 11,544 g de óxido de plomo, gastándose para ello 1,544 g de oxígeno, ¿qué porcentaje de plomo contiene la muestra, suponiendo que reacciona todo el plomo presente en la misma? -
Reaccionan 20 g de carbono y 40 g de oxígeno para formar dióxido de carbono. Si la proporción en que deben estar el carbono y el oxígeno para formar esa sustancia es de 3 : 8, ¿están las masas de carbono y oxígeno en la relación indicada en la ley de Proust? ¿Cuál de ellos sobrará? ¿Cuántos gramos de dióxido de carbono se formarán?