Q04 - Estructura Atómica
Todos los Ejercicios del Tema
Artículos de esta sección
-
-
Escribe la configuración electrónica del Na (Z = 11). ¿Cuál es la terna de números cuánticos que define el nivel energético del electrón más externo?
-
Sabiendo que el cloro tiene 17 protones en su núcleo, ¿cuáles serían las cuaternas de números cuánticos que definen a dos de los electrones más externos del átomo?
-
Indicar cuál o cuáles de los siguientes grupos de tres valores correspondientes a n, l y m son permitidos:
a) (3, -1, 1)
b) (2, 1, 3)
c) (4, 2, 0)
d) (0, 0, 0)
e) (3, 1, 1)
f) (5, 3, -3)
-
¿Puede tener un orbital los siguientes números cuánticos: n = 2; l = 2; m = 2? Razone detalladamente su respuesta.
-
Escribir la notación del orbital correspondiente a los siguientes números cuánticos: n = 4, l = 2 y m = 0.
-
Los isótopos del cobre
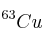
y
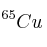
se encuentran en un porcentaje de
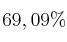
y y
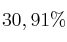
y poseen una masa atómica de 62,93 u y 64,92 u respectivamente. Determina la masa atómica media del Cu.
-
El antimonio es una mezcla de dos isótopos de masas 120,9 y 122,9. El peso atómico del antimonio es de 121,75. Hallar el tanto por ciento en abundancia natural de cada isótopo.
-
¿Cuál es la diferencia entre la estructura electrónica del ión sodio y del elemento sodio? ¿Cuál de las dos especies, el ión o el elemento, es necesaria para la salud?
YouTube Twitter

